

花粉の季節は、鼻水とくしゃみが止まらない!
「花粉症がつらい……」とお悩みのあなた、
その鼻水やくしゃみの原因は、本当に花粉だけでしょうか?
もしかしたら、ハウスダストなども原因かもしれません。
無料の検査で、アレルギーの原因を調べてみましょう!
原因が分かれば、対策も立てやすくなりますよ。
その鼻水やくしゃみの原因は、本当に花粉だけでしょうか?
もしかしたら、ハウスダストなども原因かもしれません。
無料の検査で、アレルギーの原因を調べてみましょう!
原因が分かれば、対策も立てやすくなりますよ。
年中つづく鼻水・くしゃみは 「通年性アレルギー性鼻炎」かも?
スギやヒノキの花粉は春頃に飛散しますが、ブタクサやヨモギの花粉は秋頃に飛散します。年中花粉が飛散するおかげで、花粉症の人は、ずっと鼻水やくしゃみが止まらない…。
でも、もしかしたらその症状は、ハウスダストなどが原因の「通年性アレルギー性鼻炎」かもしれません。
でも、もしかしたらその症状は、ハウスダストなどが原因の「通年性アレルギー性鼻炎」かもしれません。
「通年性アレルギー性鼻炎」って?
アレルギーの原因が花粉であれば、花粉が飛散する季節だけ症状が起きます。
でも、アレルギーの原因がハウスダストやカビであれば、季節を問わずアレルギー症状が起きます。それが「通年性アレルギー性鼻炎」です。
でも、アレルギーの原因がハウスダストやカビであれば、季節を問わずアレルギー症状が起きます。それが「通年性アレルギー性鼻炎」です。
自分のアレルゲンを、きちんと理解しましょう。
無料の検査で、まずは自分のアレルギーの原因を調べてみませんか。アレルギーの原因が分かれば、対策も立てやすくなります。アレルギー検査では、ハウスダスト、ダニ、花粉など
 代表的な8項目(※1)のアレルゲンを調べます。
代表的な8項目(※1)のアレルゲンを調べます。
治験に特化した医療機関で、親切&丁寧な検査が受けられます!もしも「通年性アレルギー性鼻炎」なら、「通年性アレルギー性鼻炎」の治験に参加することができます。
治験に参加すると、開発中の新薬を試すことができるほか、約40項目(※2)を調べる詳しい健康診断も受けられますよ。
 代表的な8項目(※1)のアレルゲンを調べます。
代表的な8項目(※1)のアレルゲンを調べます。
治験に特化した医療機関で、親切&丁寧な検査が受けられます!もしも「通年性アレルギー性鼻炎」なら、「通年性アレルギー性鼻炎」の治験に参加することができます。
治験に参加すると、開発中の新薬を試すことができるほか、約40項目(※2)を調べる詳しい健康診断も受けられますよ。
※1)アレルギー検査8項目
ハウスダスト1、ヤケヒョウヒダニ、スギ、ヒノキ、ハンノキ、カモガヤ、ブタクサ、動物上皮
※2)検診項目約40項目
中性脂肪、HDLコレステロール、LDLコレステロール、総蛋白、アルブミン、A/G、総ビリルビン、AST(GOT)、ALT(GPT)γ-GTP、LDH、ALP、コリンエステラーゼ、アミラーゼ、血糖、HbA1c(NGSP)、尿酸、Ca(カルシウム)、P(無機リン)、Na(ナトリウム)、K(カリウム)、C(l クロール)、CPK、赤血球数、ヘモグロビン濃度、ヘマトクリット値、血小板数、白血球数、好中球比、好酸球比、リンパ球比、好塩基球比、単球比、クレアチニン、CRP、血圧、身長、体重
治験に参加すると、 負担軽減費を受け取ることができます。
通年性アレルギー性鼻炎の治験に参加してくださった方には、負担軽減費をお支払いします。
負担軽減費とは、指定された日に通院したり、日常生活上のきまりを守ったり、定期的に薬を服用するなど、治験のためにさまざまなご協力をしてくださったことに対して、支払われるものです。
金額は場合によって異なりますが、おおむね1来院につき1万円程度です。
負担軽減費とは、指定された日に通院したり、日常生活上のきまりを守ったり、定期的に薬を服用するなど、治験のためにさまざまなご協力をしてくださったことに対して、支払われるものです。
金額は場合によって異なりますが、おおむね1来院につき1万円程度です。
治験ってなに?
治験とは、健康な方や患者さんの協力によって薬の候補の
効果と安全性を確かめる試験のことです。
病院で処方される薬も、ドラッグストアで手に入る薬も、
すべて、治験によって効果と安全性が確認されたものです。
薬の誕生には、10~15年という年月がかかります。
さまざまな化合物から薬の候補を見つけ、治験を行い、
国の審査をパスしたものが、やっと私たちの手元に届くのです。
効果と安全性を確かめる試験のことです。
病院で処方される薬も、ドラッグストアで手に入る薬も、
すべて、治験によって効果と安全性が確認されたものです。
薬の誕生には、10~15年という年月がかかります。
さまざまな化合物から薬の候補を見つけ、治験を行い、
国の審査をパスしたものが、やっと私たちの手元に届くのです。
ご協力いただける方、募集中!
【小学生のお子様対象】アレルギー性鼻炎のお薬モニター(大阪)
| 問い合わせ番号 | 5624 |
|---|---|
| 実施地区 | 近畿 |
| 説明 | 7歳から11歳の小学生の鼻炎症状が認められるお子様を対象としたお薬モニターです。 一定の鼻炎症状が認められるお子様を対象に、錠剤タイプのお薬を13週間服用いただいた際の効果と安全性を確認します。 参加期間:約16週間 通院回数:8回 (いずれも土日の日程となります) 実施医療機関:大阪市淀川区 モニター開始時期:2024年7月~ |
以下の全てに該当する方 ・年齢7歳以上11歳以下(性別不問) ・1年を通じて鼻炎症状が継続して認められる方 ※その他の条件により、ご参加頂けない場合があります |
|
以下のいずれかに該当する方 ①鼻茸、鼻中隔湾曲症、副鼻腔炎を合併している方 ②保護者同伴での通院が不可能な方 ※その他条件により、ご参加いただけない場合があります |
|
| 募集期限 |
【花粉症】スギ花粉による鼻炎症状のある方(関西)
| 問い合わせ番号 | 3698 |
|---|---|
| 実施地区 | |
| 説明 | 参加開始時期:2016年2月 参加期間:約2週間 内容:通院4回程度 実施施設:大阪府吹田市 この治験で使用された治験薬は、2018年1月19日に「アレサガテープ4mg・アレサガテープ8mg」として販売承認されました。 |
| ご協力いただける方 | 年齢16歳以上65歳未満(男女不問)で、以下の条件に該当する方 ※但し、未成年については、必ず親権者と一緒に通院できる方のみ参加可 ①2年以上前からスギ花粉飛散時期に鼻炎症状(鼻づまり、鼻水、くしゃみ)がある方 ②一定期間(治験開始1週間前から終了まで)、治験薬以外の鼻炎治療薬など治験薬の評価に影響がある薬剤について、使用を制限できる方 |
| ご協力いただけない方 | 以下のいずれかに該当する方 ①気管支喘息を合併している方 ②副鼻腔炎、鼻茸、鼻中隔弯曲症などの鼻疾患を合併している方 ③減感作療法や変調療法(ワクチン療法など)で治療中の方 ④狭心症・心筋梗塞などの心疾患、脳卒中などの脳血管障害の既往がある方 ⑤明らかな肝障害・腎障害を有する方 ⑥悪性腫瘍の既往または合併のある方 ⑦他の治験に参加中の方もしくは治験開始より4ヶ月以内に治験へ参加された方 ⑧妊娠中もしくは治験期間中に妊娠予定のある女性 ※その他条件により、ご参加いただけない場合があります。 |
| 募集期限 | 2016-03-20T00:00:00+09:00 |
【花粉症】スギ花粉による鼻炎症状のある方(関東)
| 問い合わせ番号 | 3697 |
|---|---|
| 実施地区 | |
| 説明 | 参加開始時期:2016年2月 参加期間:約2週間 内容:通院4回程度 実施施設:東京都新宿区、東京都小金井橋市 この治験で使用された治験薬は、2018年1月19日に「アレサガテープ4mg・アレサガテープ8mg」として販売承認されました。 |
| ご協力いただける方 | 年齢16歳以上65歳未満(男女不問)で、以下の条件に該当する方 ※但し、未成年については、必ず親権者と一緒に通院できる方のみ参加可 ①2年以上前からスギ花粉飛散時期に鼻炎症状(鼻づまり、鼻水、くしゃみ)がある方 ②一定期間(治験開始1週間前から終了まで)、治験薬以外の鼻炎治療薬など治験薬の評価に影響がある薬剤について、使用を制限できる方 |
| ご協力いただけない方 | 以下のいずれかに該当する方 ①気管支喘息を合併している方 ②副鼻腔炎、鼻茸、鼻中隔弯曲症などの鼻疾患を合併している方 ③減感作療法や変調療法(ワクチン療法など)で治療中の方 ④狭心症・心筋梗塞などの心疾患、脳卒中などの脳血管障害の既往がある方 ⑤明らかな肝障害・腎障害を有する方 ⑥悪性腫瘍の既往または合併のある方 ⑦他の治験に参加中の方もしくは治験開始より4ヶ月以内に治験へ参加された方 ⑧妊娠中もしくは治験期間中に妊娠予定のある女性 ※その他条件により、ご参加いただけない場合があります。 |
| 募集期限 | 2016-08-31T00:00:00+09:00 |
【アレルギー性鼻炎】季節問わず鼻炎症状のある方対象(関西)
| 問い合わせ番号 | 3634 |
|---|---|
| 実施地区 | |
| 説明 | 参加開始時期:2015年8月 参加期間:12週間(最大52週間まで期間延長) 内容:通院6回(最大16回) 実施施設:大阪市淀川区 この治験で使用された治験薬は、2018年1月19日に「アレサガテープ4mg・アレサガテープ8mg」として販売承認されました。 |
| ご協力いただける方 | 年齢20歳以上75歳以下(男女不問)の方、以下の条件に該当する方 ①2年以上前から季節問わず年間通じて鼻炎症状のある方 ②一定期間(治験開始から終了まで)、治験薬以外の鼻炎治療薬など治験薬の評価に影響がある薬剤について、使用を制限できる方 |
| ご協力いただけない方 | 以下のいずれかに該当する方 ①気管支喘息を合併している方 ②副鼻腔炎、鼻茸、鼻中隔弯曲症などの鼻疾患を合併している方 ③減感作療法や変調療法(ワクチン療法など)で治療中の方 ④狭心症・心筋梗塞などの心疾患、脳卒中などの脳血管障害の既往がある方 ⑤明らかな肝障害・腎障害を有する方 ⑥悪性腫瘍の既往または合併のある方 ⑦他の治験に参加中の方 ⑧妊娠中もしくは治験期間中に妊娠予定のある女性 ※その他条件により、ご参加いただけない場合があります。 |
| 募集期限 | 2017-04-30T00:00:00+09:00 |
【アレルギー性鼻炎】季節問わず鼻炎症状のある方対象(関東)
| 問い合わせ番号 | 3607 |
|---|---|
| 実施地区 | |
| 説明 | 参加開始時期:2015年8月 参加期間:12週間(最大52週間まで期間延長) 内容:通院6回(最大16回) 実施施設、東京都新宿区、東京都小金井橋市 この治験で使用された治験薬は、2018年1月19日に「アレサガテープ4mg・アレサガテープ8mg」として販売承認されました。 |
| ご協力いただける方 | 年齢20歳以上75歳以下(男女不問)の方、以下の条件に該当する方 ①2年以上前から季節問わず年間通じて鼻炎症状のある方 ②一定期間(治験開始から終了まで)、治験薬以外の鼻炎治療薬など治験薬の評価に影響がある薬剤について、使用を制限できる方 |
| ご協力いただけない方 | 以下のいずれかに該当する方 ①気管支喘息を合併している方 ②副鼻腔炎、鼻茸、鼻中隔弯曲症などの鼻疾患を合併している方 ③減感作療法や変調療法(ワクチン療法など)で治療中の方 ④狭心症・心筋梗塞などの心疾患、脳卒中などの脳血管障害の既往がある方 ⑤明らかな肝障害・腎障害を有する方 ⑥悪性腫瘍の既往または合併のある方 ⑦他の治験に参加中の方 ⑧妊娠中もしくは治験期間中に妊娠予定のある女性 ※その他条件により、ご参加いただけない場合があります。 |
| 募集期限 | 2015-10-31T00:00:00+09:00 |
【アレルギー性鼻炎】大募集!! 今年夏より実施 短期通院試験(関西)
| 問い合わせ番号 | 3463 |
|---|---|
| 実施地区 | |
| 説明 | 試験開始時期:2014年8月 参加期間:約1ヵ月半(6~7週間) 内容:通院5回 実施施設:大阪市淀川区 この治験で使用された治験薬は、2016年9月28日に「ビラノア錠20mg」として販売承認されました。 |
| ご協力いただける方 | 年齢18歳以上64歳以下(男女不問)の方で、以下の条件に該当する方 ※未成年の方は保護者と一緒に通院できる方が参加条件となります ①季節を問わず年中鼻炎症状(鼻づまり、鼻水、くしゃみ)がある方 ②一定期間(治験開始2週間前から終了まで)、治験薬以外の鼻炎治療薬など 治験薬の評価に影響がある薬剤について、使用を制限できる方 ③女性の場合は、閉経している方もしくは適切な避妊を実施いただける方 |
| ご協力いただけない方 | 以下のいずれかに該当する方 ①花粉(スギ、ヒノキ、イネ科、ヨモギ属、ブタクサ属等)をアレルゲンとして保持しており、 治験参加時期がその飛散期にあたる方 ②気管支喘息を合併している方 ③副鼻腔炎、鼻茸、鼻中隔弯曲症などの鼻疾患を合併している方 ④減感作療法や変調療法(ワクチン療法など)で治療中の方 ⑤狭心症・心筋梗塞などの心疾患、脳卒中などの脳血管障害の既往がある方 ⑥明らかな肝障害・腎障害を有する方 ⑦悪性腫瘍の既往または合併のある方 ⑧他の治験に参加中の方 ※その他条件により、ご参加いただけない場合があります。 |
| 募集期限 | 2015-01-04T00:00:00+09:00 |
【花粉症】関西地区限定!初夏から開始 長期通院試験
| 問い合わせ番号 | 3462 |
|---|---|
| 実施地区 | |
| 説明 | 通年性及び季節性アレルギー性鼻炎患者を対象とした長期投与試験のご案内です。 参加開始時期:2014年8月 参加期間:約3ヵ月間(最大1年間まで) 内容:通院6回(最大16回まで) 実施施設:大阪市淀川区 この治験で使用された治験薬は、2016年9月28日に「ビラノア錠20mg」として販売承認されました。 |
| ご協力いただける方 | 年齢20歳以上64歳以下(男女不問)の方で、以下の条件に該当する方 ①季節を問わず年中鼻炎症状(鼻づまり、鼻水、くしゃみ)がある方 ②一定期間(治験開始2週間前から終了まで)、治験薬以外の鼻炎治療薬など治験薬の評価に影響がある薬剤について、使用を制限できる方 ③女性の場合は、閉経している方もしくは適切な避妊を実施いただける方 |
| ご協力いただけない方 | 以下のいずれかに該当する方 ①花粉(スギ、ヒノキ、イネ科、ヨモギ属、ブタクサ属等)をアレルゲンとして保持しており、治験参加時期がその飛散期にあたる方 ②気管支喘息を合併している方 ③副鼻腔炎、鼻茸、鼻中隔弯曲症などの鼻疾患を合併している方 ④減感作療法や変調療法(ワクチン療法など)で治療中の方 ⑤狭心症・心筋梗塞などの心疾患、脳卒中などの脳血管障害の既往がある方 ⑥明らかな肝障害・腎障害を有する方 ⑦悪性腫瘍の既往または合併のある方 ⑧他の治験に参加中の方 ※その他条件により、ご参加いただけない場合があります。 |
| 募集期限 | 2014-09-20T00:00:00+09:00 |
【花粉症】関東地区限定!2月から開始の短期通院試験
| 問い合わせ番号 | 3436 |
|---|---|
| 実施地区 | |
| 説明 | 通年性及び季節性アレルギー性鼻炎患者を対象とした長期投与試験のご案内です。 参加開始時期:2015年2月 参加期間:約3ヵ月間(最大1年間まで) 内容:通院6回(最大16回まで) 実施施設:東京都新宿区 この治験で使用された治験薬は、2016年9月28日に「ビラノア錠20mg」として販売承認されました。 |
| ご協力いただける方 | 年齢20歳以上64歳以下(男女不問)の方で、以下の条件に該当する方 ①スギ花粉飛散時期に鼻炎症状(鼻づまり、鼻水、くしゃみ)がある方 ②一定期間(治験開始2週間前から終了まで)、治験薬以外の鼻炎治療薬など治験薬の評価に影響がある薬剤について、使用を制限できる方 |
| ご協力いただけない方 | 以下のいずれかに該当する方 ①気管支喘息を合併している方 ②副鼻腔炎、鼻茸、鼻中隔弯曲症などの鼻疾患を合併している方 ③減感作療法や変調療法(ワクチン療法など)で治療中の方 ④狭心症・心筋梗塞などの心疾患、脳卒中などの脳血管障害の既往がある方 ⑤明らかな肝障害・腎障害を有する方 ⑥悪性腫瘍の既往または合併のある方 ⑦他の治験に参加中の方 ⑧妊娠中もしくは治験期間中に妊娠予定のある女性 ※その他条件により、ご参加いただけない場合があります。 |
| 募集期限 | 2015-02-28T00:00:00+09:00 |
【アレルギー性鼻炎】大募集!! 今年夏より実施 短期通院試験(関西)
| 問い合わせ番号 | 3324 |
|---|---|
| 実施地区 | |
| 説明 | 試験開始時期:2014年8月 参加期間:約1ヵ月半(6~7週間) 内容:通院5回 実施施設:大阪府吹田市 この治験で使用された治験薬は、2016年9月28日に「ビラノア錠20mg」として販売承認されました。 |
| ご協力いただける方 | 年齢18歳以上64歳以下(男女不問)の方で、以下の条件に該当する方 ※未成年の方は保護者と一緒に通院できる方が参加条件となります ①季節を問わず年中鼻炎症状(鼻づまり、鼻水、くしゃみ)がある方 ②一定期間(治験開始2週間前から終了まで)、治験薬以外の鼻炎治療薬など 治験薬の評価に影響がある薬剤について、使用を制限できる方 ③女性の場合は、閉経している方もしくは適切な避妊を実施いただける方 |
| ご協力いただけない方 | 以下のいずれかに該当する方 ①花粉(スギ、ヒノキ、イネ科、ヨモギ属、ブタクサ属等)をアレルゲンとして保持しており、 治験参加時期がその飛散期にあたる方 ②気管支喘息を合併している方 ③副鼻腔炎、鼻茸、鼻中隔弯曲症などの鼻疾患を合併している方 ④減感作療法や変調療法(ワクチン療法など)で治療中の方 ⑤狭心症・心筋梗塞などの心疾患、脳卒中などの脳血管障害の既往がある方 ⑥明らかな肝障害・腎障害を有する方 ⑦悪性腫瘍の既往または合併のある方 ⑧他の治験に参加中の方 ※その他条件により、ご参加いただけない場合があります。 |
| 募集期限 | 2014-12-27T00:00:00+09:00 |
【通年性アレルギー性鼻炎】夏から冬にかけて実施予定(関西)
| 問い合わせ番号 | 3269 |
|---|---|
| 実施地区 | |
| 説明 | 試験開始時期:2013年7月 参加期間:約1ヵ月間 内容:通院5回 実施施設:大阪市淀川区 この治験で使用された治験薬は、2016年9月28日に「デザレックス錠5㎎」として販売承認されました。 |
| ご協力いただける方 | 年齢20歳以上(男女不問)の方で以下の条件に該当する方 ①季節を問わず年中鼻炎症状(くしゃみ、鼻水、鼻づまり)がある方 ②一定期間(治験開始4週間前から終了まで)、治験薬以外の鼻炎の治療薬など(治験薬の評価に影響がある薬剤)の使用を制限できる方 ③女性の場合は、閉経している方もしくは適切な避妊を実施いただける方 |
| ご協力いただけない方 | 以下のいずれかに該当する方 ①花粉(スギ、ヒノキ、イネ科、ヨモギ、ブタクサ等)をアレルゲンとして保持しており、治験参加時期がその飛散期にあたる方 ②気管支喘息を合併しており、治療中の方 ③鼻茸、鼻中隔弯曲症や感染性副鼻腔炎などの鼻疾患を合併している方 ④減感作療法や変調療法(ワクチン療法など)で治療中の方 ⑤狭心症・心筋梗塞などの心疾患、脳卒中などの脳血管障害の既往がある方 ⑥明らかな肝障害・腎障害を有する方 ⑦悪性腫瘍の既往または合併のある方 ⑧他の治験に参加中の方 ※その他条件により、ご参加いただけない場合があります。 |
| 募集期限 | 2014-01-01T00:00:00+09:00 |
【通年性アレルギー性鼻炎】夏から冬にかけて実施予定(関東)
| 問い合わせ番号 | 3241 |
|---|---|
| 実施地区 | |
| 説明 | 試験開始時期:2013年7月 参加期間:約1ヵ月間 内容:通院5回 実施施設:東京都新宿区 この治験で使用された治験薬は、2016年9月28日に「デザレックス錠5㎎」として販売承認されました。 |
| ご協力いただける方 | 年齢20歳以上(男女不問)の方で以下の条件に該当する方 ①季節を問わず年中鼻炎症状(くしゃみ、鼻水、鼻づまり)がある方 ②一定期間(治験開始4週間前から終了まで)、治験薬以外の鼻炎の治療薬など(治験薬の評価に影響がある薬剤)の使用を制限できる方 ③女性の場合は、閉経している方もしくは適切な避妊を実施いただける方 |
| ご協力いただけない方 | 以下のいずれかに該当する方 ①花粉(スギ、ヒノキ、イネ科、ヨモギ、ブタクサ等)をアレルゲンとして保持しており、治験参加時期がその飛散期にあたる方 ②気管支喘息を合併しており、治療中の方 ③鼻茸、鼻中隔弯曲症や感染性副鼻腔炎などの鼻疾患を合併している方 ④減感作療法や変調療法(ワクチン療法など)で治療中の方 ⑤狭心症・心筋梗塞などの心疾患、脳卒中などの脳血管障害の既往がある方 ⑥明らかな肝障害・腎障害を有する方 ⑦悪性腫瘍の既往または合併のある方 ⑧他の治験に参加中の方 ※その他条件により、ご参加いただけない場合があります。 |
| 募集期限 | 2014-05-05T00:00:00+09:00 |
【通年性アレルギー性鼻炎】12歳~64歳迄の鼻炎患者対象の長期投与試験(関西)
| 問い合わせ番号 | 2976 |
|---|---|
| 実施地区 | |
| 説明 | 今回は、アレルギー性鼻炎の新しい治療、「舌下投薬による減感作療法」の治験となります。 室内の塵ダニ(ハウスダスト)が原因で年中、くしゃみ・鼻水・鼻詰まりの鼻炎症状がある12歳から64歳までの男性と女性に参加いただく内容です。5252週間で4週間から8週間毎に通院いただきます。多くのご応募をお待ちしております。 試験開始時期:2012年4月 参加期間:52週間 内容:通院12回 実施施設:大阪市淀川区 この治験で使用された治験薬は、2015年9月28日に「ミティキュアダニ舌下錠3,300JAU/10,000JAU」として販売承認されました。 |
| ご協力いただける方 | 同意取得時の年齢が12歳以上65歳未満の男性と女性 季節問わず年中鼻炎症状がある方 本治験の実施の1年以上前から治療薬等で鼻炎症状の治療をしている方 ダニが原因でアレルギー性鼻炎の症状がある方 |
| ご協力いただけない方 | ダニ以外のスギ、ヒノキ、ブタクサ、イヌ、ネコなどの他のアレルギー抗体が原因でダニよりも鼻炎症状がひどい方 年中、鼻づまりの症状がある方 3年以内に鼻症状の治療のためにレーザー治療、手術を受けた方 気管支喘息の症状がある方 治験開始の12週間前に他の治験に参加していた方 |
| 募集期限 | 2014-01-23T00:00:00+09:00 |
治験はどこで?
治験は、大阪の「大阪治験病院」と「OCROMクリニック」、
東京の「ToCROMクリニック」のいずれかで行われます。
治験に特化した医療機関なので、ここに通院・入院しているのは、
原則として治験ボランティアの方のみ。
大勢の治験ボランティアを支えてきたスタッフが、
親切丁寧に対応します。
東京の「ToCROMクリニック」のいずれかで行われます。
治験に特化した医療機関なので、ここに通院・入院しているのは、
原則として治験ボランティアの方のみ。
大勢の治験ボランティアを支えてきたスタッフが、
親切丁寧に対応します。
大阪治験病院
大阪治験病院は、大阪臨床薬理研究所(OPHA Clinic)の20数年間・1,000試験を超える経験に基づくノウハウを継承して、2005年11月に開設された、日本初の治験に特化した病院です。大阪治験病院は53床のベッドを有し、第I相試験から製造販売後臨床試験までの治験の実施が可能な病院です。新大阪駅から徒歩5分という好立地にあります。

〒532-0003 大阪府大阪市淀川区宮原4-1-29 TEL:06-6395-9000 JR・地下鉄新大阪駅より徒歩5分
OCROMクリニック
1999年に開設されたOCROMクリニックは、日本初の外来治験専門医療機関です。クリニックのある桃山台(大阪府吹田市)は、緑が豊かで落ち着いた環境が特色です。外来患者試験や、健康な方を対象にした試験はもちろん、宿泊が必要な臨床薬理試験も実施できるクリニックとして利用されています。

〒565-0853 大阪府吹田市春日4-12-11 千里サンプラザ TEL:06-6330-8810 北大阪急行電鉄 桃山台駅 徒歩12分
ToCROMクリニック
東京都新宿区にあるToCROMクリニックは、一般診療も可能な治験実施医療機関です。外来患者試験だけでなく、宿泊を伴うPK/PD試験(薬力学試験)も実施できる点が特色です。2000年に開設されて以来、主に生活習慣病の領域で、さまざまな実績を残しています。
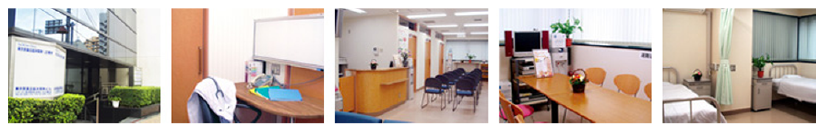
〒160-0008 東京都新宿区三栄町17-10 TEL:03-5366-5333 四ツ谷駅徒歩7分、四谷三丁目駅徒歩8分
ボランティアの声
岩崎雅明さん
花粉症の人を対象にした治験に参加しました。3年ほど前、知人が「花粉症の新薬を試す機会があるよ」と、治験について教えてくれました。「花粉症が治ったらいいなぁ」と考えた私は、気軽な気持ちで治験に参加することにしました。
続きはこちら>>
続きはこちら>>

太田瞳さん
アレルギー性鼻炎は子どものときからで、季節の変わり目などにひどくなると鼻からのどにきて、扁桃腺が腫れて熱がでるんです。大人になってからも、会議や試験中にくしゃみが止まらなくなって退出し...
続きはこちら>>
続きはこちら>>

説明会・治験参加の流れ

STEP.1Webまたはフリーダイヤルからお申し込み
治験に興味をもった方は
まずボランティア登録説明会(無料)に予約申し込みをしてください。
まずボランティア登録説明会(無料)に予約申し込みをしてください。


STEP.2登録説明会に参加
登録説明会では、担当者から治験の目的や内容、
メリット・デメリットを説明しますので、治験に対する理解を深めてから
登録手続きをしてください。
メリット・デメリットを説明しますので、治験に対する理解を深めてから
登録手続きをしてください。


STEP.3健康診断の受診
(フェーズ2&3試験の場合のみ)
治験実施医療機関にて健康診断を受けていただきます。


STEP.4治験説明会に参加
治験実施医療機関においてご希望の治験について詳細な説明があります。
十分にご理解いただけましたら、治験参加同意書にご署名ください。
十分にご理解いただけましたら、治験参加同意書にご署名ください。


STEP.5治験参加
事前にお知らせしたスケジュールに沿って、治験実施医療機関にお越しください。
いよいよ治験のスタートです。
いよいよ治験のスタートです。
ボランティアの声
インクロムは、1983年に初めて治験事業に携わって以来、1,600件以上の治験に携わってきました。 その中で、実際に商品化された医薬品は48件※にのぼります(※平成20年1月~平成24年12月に承認されたもの。 平心会3施設で関与した部会審議品目)。これまでに開発をサポートした医薬品は、病院で投与・処方される糖尿病、高血圧症、 脂質異常症の薬をはじめ、インフルエンザの抗ウイルス薬、C型肝炎の薬やドラッグストアで購入できる目薬や花粉症の薬など、多岐に渡ります。
花粉症を含むアレルギー性鼻炎の薬に関しては、40件以上の試験に携わり、のべ4000名以上の方にご協力をいただいています。 現在も、多くの治験ボランティアの方々と共に、さまざまな薬の開発に携わっています。
花粉症を含むアレルギー性鼻炎の薬に関しては、40件以上の試験に携わり、のべ4000名以上の方にご協力をいただいています。 現在も、多くの治験ボランティアの方々と共に、さまざまな薬の開発に携わっています。
インクロムは、治験をより多くの方に知ってもらうために、その啓発活動にも力を入れています。 治験は、医薬品の開発にはなくてはならないプロセスですが、大勢の方に知られているとはいえないのが現状です。
インクロムでは、医薬の進歩に貢献するためにも、治験の理解を広げる活動が不可欠だと考えています。
◇テレビCM「おくすりボランティア」
2013年2月から、治験を知ってもらうためのテレビCMを放送しています(関西のみ)。この作品は、日本において、民間企業が初めて放送した治験啓発CMです。
◇PRキャラクター「神農さま」
治験をPRするオリジナルキャラクター。地域のイベントなどに参加し、幅広い年齢層の方に治験を知ってもらう活動を行っています。
インクロムでは、医薬の進歩に貢献するためにも、治験の理解を広げる活動が不可欠だと考えています。
◇テレビCM「おくすりボランティア」
2013年2月から、治験を知ってもらうためのテレビCMを放送しています(関西のみ)。この作品は、日本において、民間企業が初めて放送した治験啓発CMです。
◇PRキャラクター「神農さま」
治験をPRするオリジナルキャラクター。地域のイベントなどに参加し、幅広い年齢層の方に治験を知ってもらう活動を行っています。
インクロムの特長は、医療法人平心会と提携していることです。 インクロムで行われる治験は、平心会に所属する3医療機関のいずれかで行われます。 医療法人平心会に属する「大阪治験病院」「OCROMクリニック」「ToCROMクリニック」は、いずれも治験に特化した医療機関です。 大勢の治験ボランティアを支えてきた「治験のプロ」が、ていねいな対応を行います。





